Les dispositifs implantables sont définis au règlement européen (UE) RDM 2017/745 (chapitre 1er, article 2, alinéa 5)
La France impose la traçabilité tous les dispositifs implantables via le décret 2026-299 du 17 avril 2026 (section 5, articles R. 5212-33, -34, -45 du CSP), notamment pour :
- Les dispositifs implantables stériles ou stérilisables (sauf ceux exemptés car hors contact avec des zones critiques) ;
- Certains produits sans destination médicale, notamment ceux à visée esthétique,
- Les dispositifs inscrits sur une liste arrêtée par le directeur de l’ANSM.
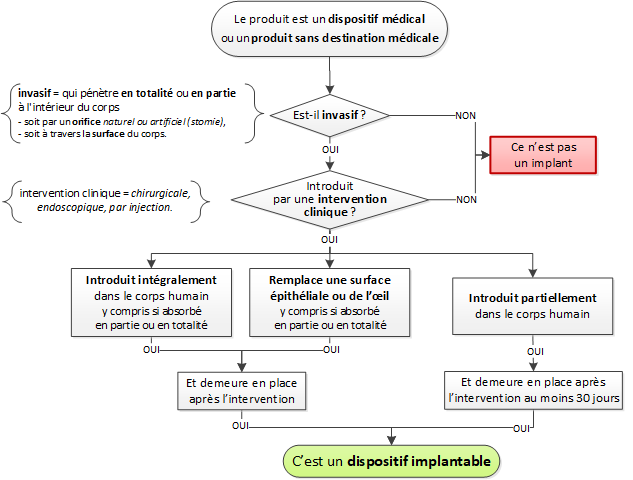
Traçabilité des dispositifs implantables
![]() Quels sont les dispositifs implantables soumis à traçabilité obligatoire ? (fiche de bonnes pratiques – mai 2026)
Quels sont les dispositifs implantables soumis à traçabilité obligatoire ? (fiche de bonnes pratiques – mai 2026) ![]()
![]() Décret 2026-299 du 17 avril 2026 : règles de traçabilité (Journal officiel)
Décret 2026-299 du 17 avril 2026 : règles de traçabilité (Journal officiel)
Management de la qualité du circuit des dispositifs implantables
![]() Arrêté du 8 septembre 2021 relatif au management de la qualité du circuit des dispositifs implantables dans les établissements de santé et les installations de chirurgie esthétique (Ministère ; Texte officiel – septembre 2021)
Arrêté du 8 septembre 2021 relatif au management de la qualité du circuit des dispositifs implantables dans les établissements de santé et les installations de chirurgie esthétique (Ministère ; Texte officiel – septembre 2021)
![]() Maîtrise de la qualité du circuit des dispositifs implantables : trame type du bilan annuel du RSMQ (fiche de bonnes pratiques – mars 2022)
Maîtrise de la qualité du circuit des dispositifs implantables : trame type du bilan annuel du RSMQ (fiche de bonnes pratiques – mars 2022)
![]() Fiche de poste du RSMQ responsable du système de management de la qualité du circuit des dispositifs implantables (OMéDITs Bretagne, Centre Val de Loire, Normandie, Pays de la Loire ; fiche de bonnes pratiques – juillet 2023)
Fiche de poste du RSMQ responsable du système de management de la qualité du circuit des dispositifs implantables (OMéDITs Bretagne, Centre Val de Loire, Normandie, Pays de la Loire ; fiche de bonnes pratiques – juillet 2023)
![]() Prothèses explantées : méthodes de conservation ou destruction (fiche de bonnes pratiques – avril 2026)
Prothèses explantées : méthodes de conservation ou destruction (fiche de bonnes pratiques – avril 2026) ![]()
Web-séries DMI
Le réseau des OMEDIT organise des webinaires autour de l’informatisation du circuit des dispositifs médicaux implantables : Web-série DMI « Pour optimiser le circuit des DMI : l’interopérabilité c’est la clé. Mais par où commencer ? ».
Au cours de chaque webinaire, une thématique est abordée avec le partage d’expérience de 2 établissements de santé de deux régions suivis d’échanges avec les participants.
Vous trouverez ici les liens pour revoir en replay les Webinaires passés :
![]() Web-série DMI – Saison1 Episode 1 – « Peut-on atteindre 100% de traçabilité sanitaire des DMI en temps réel ? » (Résomédit ; webinaire – janvier 2024)
Web-série DMI – Saison1 Episode 1 – « Peut-on atteindre 100% de traçabilité sanitaire des DMI en temps réel ? » (Résomédit ; webinaire – janvier 2024)
![]() Web-série DMI – Saison 1 Episode 2 – « PUI – bloc opératoire : une communication à double sens ? » (Résomédit ; webinaire – février 2024)
Web-série DMI – Saison 1 Episode 2 – « PUI – bloc opératoire : une communication à double sens ? » (Résomédit ; webinaire – février 2024)
![]() Web-série DMI – Saison 1 Episode 3 – « Au commencement…était le référencement » (Résomédit ; webinaire – mars 2024)
Web-série DMI – Saison 1 Episode 3 – « Au commencement…était le référencement » (Résomédit ; webinaire – mars 2024)
![]() Web Série DMI – Saison 1 Episode 4 – « Quid de la gestion de stock au bloc » (Résomédit ; webinaire – juin 2024)
Web Série DMI – Saison 1 Episode 4 – « Quid de la gestion de stock au bloc » (Résomédit ; webinaire – juin 2024)
![]() Web Série DMI – Saison 1 Episode 5 – « Remise du document de traçabilité des DMI au patient » (Résomédit ; webinaire – octobre 2024)
Web Série DMI – Saison 1 Episode 5 – « Remise du document de traçabilité des DMI au patient » (Résomédit ; webinaire – octobre 2024)
![]() Web Série DMI – Saison 1 Episode 6 – « Armoires sécurisées dédiées aux DMI » (Résomédit ; webinaire – novembre 2024)
Web Série DMI – Saison 1 Episode 6 – « Armoires sécurisées dédiées aux DMI » (Résomédit ; webinaire – novembre 2024)
![]() Web Série DMI – Saison 2 Episode 1 – « Recueil des indications de pose de DMI et actions de pharmacie clinique » (Résomédit ; webinaire – janvier 2025)
Web Série DMI – Saison 2 Episode 1 – « Recueil des indications de pose de DMI et actions de pharmacie clinique » (Résomédit ; webinaire – janvier 2025)
![]() Web Série DMI – Saison 2 Episode 2 – « Pertinence et bon usage des DMI au bénéfice du patient : quels leviers ? » (Résomédit ; webinaire – mars 2025)
Web Série DMI – Saison 2 Episode 2 – « Pertinence et bon usage des DMI au bénéfice du patient : quels leviers ? » (Résomédit ; webinaire – mars 2025)




