Les DM sont des produits de santé utilisés chez l’homme (implants, équipements, consommables, etc.) utilisés pour compenser un handicap ou une blessure, atténuer une maladie, ou pour une finalité diagnostique ou thérapeutique, ou comme moyen de maitrise de la conception.
Ils agissent selon un mécanisme d’action dit « mécanique », c’est-à-dire qui n’est ni pharmacologique, ni immunologique, ni métabolique.
Leur mise sur le marché se fait sous la responsabilité du fabricant. Elle dépend du règlement européen RDM 2017/745. Leur conformité est matérialisée en Europe par le marquage CE médical qui garantit que le dispositif médical répond à des exigences de sécurité, de performance et de bénéfice clinique.
Le mode de démonstration de la conformité à ces exigences est d’autant plus contraignant que la classe de risque du DM est élevée.
Etiquetage des dispositifs médicaux
![]() Pictogrammes des dispositifs médicaux : symboles retrouvés sur les emballages (fiche de bonnes pratiques – novembre 2023)
Pictogrammes des dispositifs médicaux : symboles retrouvés sur les emballages (fiche de bonnes pratiques – novembre 2023)
![]() Connaître les symboles (« pictogrammes ») des dispositifs médicaux (e-learning – mars 2024)
Connaître les symboles (« pictogrammes ») des dispositifs médicaux (e-learning – mars 2024)
![]() Audit sur le stockage et l’étiquetage des dispositifs médicaux stériles (grille d’audit – mars 2020)
Audit sur le stockage et l’étiquetage des dispositifs médicaux stériles (grille d’audit – mars 2020)
Management de la qualité du circuit des DM
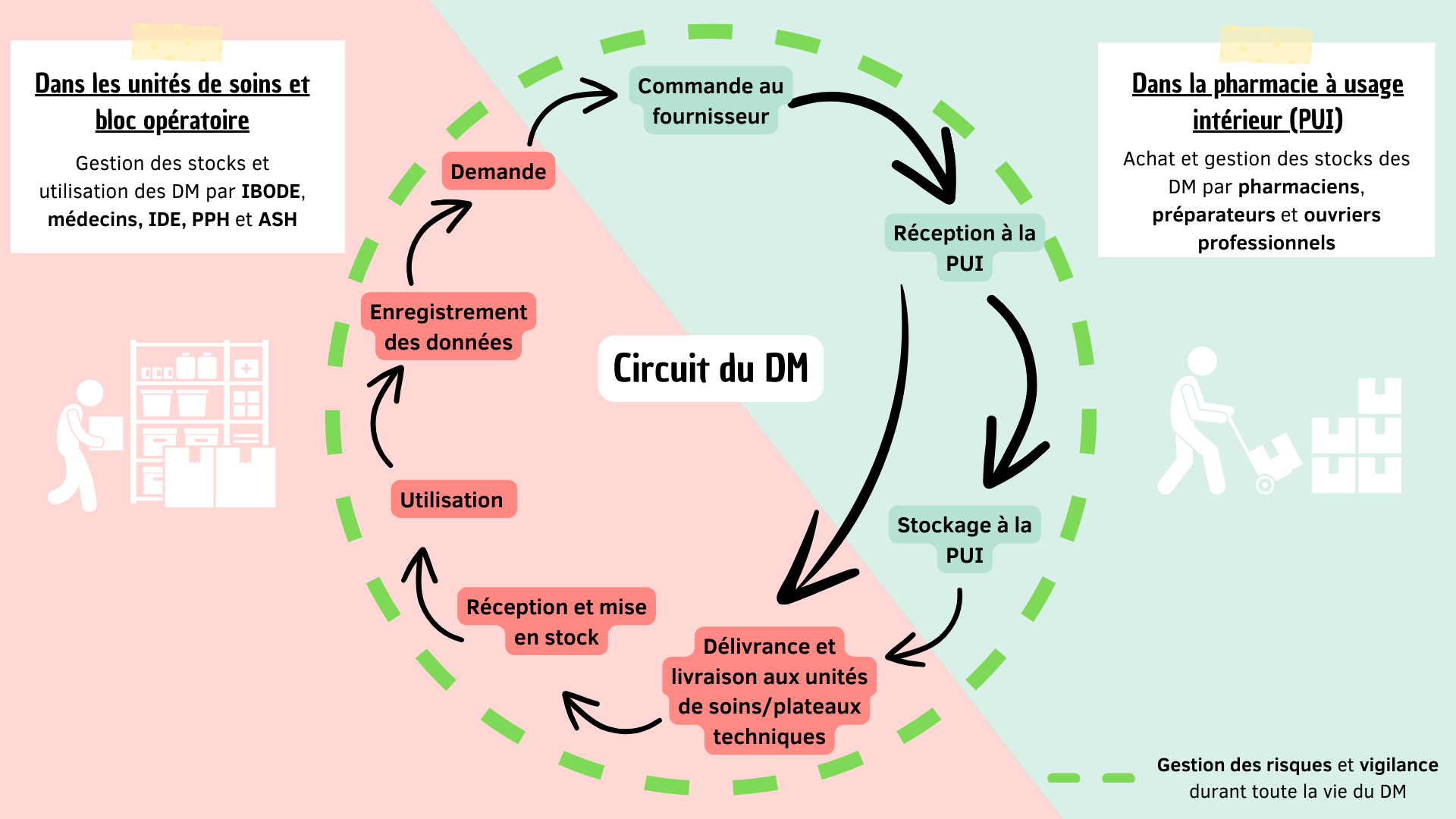
Règlementation française
Art. L6111-2 du CSP : Les établissements élaborent et mettent en œuvre une politique d’amélioration continue de la qualité et de la sécurité des soins et une gestion des risques visant à prévenir et traiter les EI liés à leurs activités. Dans ce cadre, ils définissent une politique […] des DM stériles et mettent en place un système qualité […] de la stérilisation des DM
Art. R6144 -2 et -3 : La CME ou la CfME contribue à l’élaboration de la politique d’amélioration continue de la qualité et de la sécurité des soins, notamment en ce qui concerne la gestion globale et coordonnée des risques, les dispositifs de vigilance destinés à garantir la sécurité sanitaire, la politique des DM stériles […]
![]() Décret n° 2026-299 du 17 avril 2026 relatif aux dispositifs médicaux (Ministère ; Texte officiel – avril 2026)
Décret n° 2026-299 du 17 avril 2026 relatif aux dispositifs médicaux (Ministère ; Texte officiel – avril 2026) ![]()
![]() Arrêté du 8 septembre 2021 relatif au management de la qualité du circuit des dispositifs médicaux implantables dans les établissements de santé et les installations de chirurgie esthétique (Ministère ; Texte officiel – septembre 2021)
Arrêté du 8 septembre 2021 relatif au management de la qualité du circuit des dispositifs médicaux implantables dans les établissements de santé et les installations de chirurgie esthétique (Ministère ; Texte officiel – septembre 2021)
Règlementation européenne, marquage CE
![]() RDM : Règlement (UE) 2017/745 sur les dispositifs médicaux (Parlement européen ; texte officiel – mai 2017)
RDM : Règlement (UE) 2017/745 sur les dispositifs médicaux (Parlement européen ; texte officiel – mai 2017)
Aux côtés de la gouvernance européenne siège le groupe de coordination des DM (MDCG) (art. 103 et 105 du RDM) qui produit des textes qui éclairent les actes d’exécution du règlement RDM.
Réduction des risques
![]() Bon usage des colorants utilisés au et hors bloc opératoire (fiche de bonnes pratiques – mars 2026)
Bon usage des colorants utilisés au et hors bloc opératoire (fiche de bonnes pratiques – mars 2026)
![]() Quels sont les dispositifs implantables soumis à traçabilité obligatoire ? (fiche de bonnes pratiques – mai 2026)
Quels sont les dispositifs implantables soumis à traçabilité obligatoire ? (fiche de bonnes pratiques – mai 2026) ![]()
![]() INF’OMéDIT : focus sur les outils pour sécuriser le circuit des dispositifs médicaux (synthèse documentaire – décembre 2023)
INF’OMéDIT : focus sur les outils pour sécuriser le circuit des dispositifs médicaux (synthèse documentaire – décembre 2023)
![]() Liste des Never Events DM : 10 situations à risque liées aux dispositifs médicaux stériles, évitables (Euro-Pharmat ; liste – juin 2021)
Liste des Never Events DM : 10 situations à risque liées aux dispositifs médicaux stériles, évitables (Euro-Pharmat ; liste – juin 2021)
Flash sécurité patient FSP (HAS) : voir la page dédiée de la Haute Autorité de Santé
Pour chacun des cas abordés, il est proposé en plus du document de synthèse : le contexte, l’objectif du flash, et les principales recommandations pour que cela ne se reproduise pas.
- Patient trachéotomisé en service de soins critiques (HAS ; FSP – février 2024)
- Les dispositifs implantables (DI) : Implanter sans se planter (HAS ; FSP – décembre 2023)
- Cathéters et infections associées aux soins : Trop longtemps il restera, une infection tu risqueras (HAS ; FSP – novembre 2023)
- Changement de sonde nasogastrique chez l’adulte : Une mauvaise position et c’est la réanimation (HAS ; FSP – septembre 2022)
- Dispositifs médicaux (Mauvais réglage, erreur de calcul ou de programmation, surdosage,…) (HAS ; FSP – novembre 2021)
Euro-Pharmat propose 26 fiches actions de réduction des risques (livret du DM, substitution d’un DM, mise en place de référents, bonnes pratiques de stockage, bonnes pratiques de transport, dotation d’une unité de soins, audit des stocks dans les unités de soins…)
![]() Maintenance et contrôle qualité des dispositifs médicaux (ANSM ; documents de référence – mai 2021)
Maintenance et contrôle qualité des dispositifs médicaux (ANSM ; documents de référence – mai 2021)
Sécurisation des pratiques
![]() Calcul de dose : l’essentiel (mémo – mai 2022)
Calcul de dose : l’essentiel (mémo – mai 2022)
NB : document à imprimer en recto-verso et à plier en 3, de manière à obtenir un dépliant 3 volets
![]() Bonnes pratiques professionnelles des Prestataires de Services et Distributeurs de Matériel (PSDM) (HAS ; guide méthodologique – juin 2024)
Bonnes pratiques professionnelles des Prestataires de Services et Distributeurs de Matériel (PSDM) (HAS ; guide méthodologique – juin 2024)
![]() Prescription Hospitalière et bonne dispensation en Ville – Pansements (Euro-Pharmat ; cahier de prescription et dispensation – mars 2020)
Prescription Hospitalière et bonne dispensation en Ville – Pansements (Euro-Pharmat ; cahier de prescription et dispensation – mars 2020)
![]() Prescription Hospitalière et bonne dispensation en Ville – Perfusion (Euro-Pharmat ; cahier de prescription et dispensation – mars 2022)
Prescription Hospitalière et bonne dispensation en Ville – Perfusion (Euro-Pharmat ; cahier de prescription et dispensation – mars 2022)
![]() Prescription Hospitalière et bonne dispensation en Ville – Stomathérapie (Euro-Pharmat ; cahier de prescription et dispensation – mai 2023)
Prescription Hospitalière et bonne dispensation en Ville – Stomathérapie (Euro-Pharmat ; cahier de prescription et dispensation – mai 2023)
![]() Prescription Hospitalière et bonne dispensation en Ville – Diabétologie (Euro-Pharmat ; cahier de prescription et dispensation – mai 2022)
Prescription Hospitalière et bonne dispensation en Ville – Diabétologie (Euro-Pharmat ; cahier de prescription et dispensation – mai 2022)




